Plomo
Ficha técnica
El plomo es un metal blando, maleable, dúctil y de color gris azulado. La mayor parte del plomo presente en la atmósfera se encuentra en forma de partículas de diámetro menor de una micra.
Es muy peligroso para el medio ambiente debido a su elevada toxicidad. No se degrada ni química ni biológicamente por la naturaleza, lo que provoca que permanezca en ella durante un largo periodo de tiempo; esto afecta muy gravemente a las cadenas tróficas, debido a la acumulación de plomo en los organismos de los seres vivos (bioacumulación).
Se encuentra en muy bajas concentraciones en la atmósfera, sin embargo, la extracción de plomo de las minas, el refinado, el amplio uso industrial y la combustión de gasolinas han contribuido al aumento de su concentración en el aire, principalmente en zonas urbanas y mineras.
Efectos
Este metal se utiliza mucho en la industria debido a sus magníficas propiedades químicas, sin embargo, su utilización debe llevarse a cabo bajo estrictas medidas de seguridad, ya que a altas concentraciones puede ser nocivo para la salud.
Salud
En general, el plomo a elevadas concentraciones puede producir efectos perjudiciales en la salud.
Vegetación
En la vegetación el plomo se acumula principalmente en las hojas por la deposición atmosférica y depende de la distancia de las plantas a la fuente de emisión.
Se absorbe bien porque el plomo presente en la hoja rompe la cutícula y pasa al interior de la misma, se acumula en las vesículas y pude originar efectos como los indicados a continuación.
- Inhibición de la mitosis y por tanto del crecimiento de la planta.
- Inhibición de la síntesis del ATP y del rendimiento energético.
- Disminución de la viabilidad de las semillas.
Fuentes
Naturales
La contribución de las fuentes naturales a la concentración ambiental de plomo es muy reducida y sin importancia a efectos de posible intoxicación. Entre las aportaciones naturales podemos destacar las originadas por incendios y emisiones volcánicas.
Antropogénicas
En las áreas industriales la contaminación de plomo es mucho más elevada debido a los usos industriales de este elemento y de sus derivados. Entre los procesos industriales que utilizan el plomo podemos citar las industrias químicas (pinturas, esmaltes,...), industrias mineras, procesos de fundición y recuperación de metales, la incineración de residuos, fangos de depuración y la combustión de las gasolinas con plomo.
El transporte (vehículos con motor a gasolina) ha sido durante muchos años la mayor fuente de emisión de plomo, al ser empleado como aditivo antidetonante de la gasolina en forma de tetraetilo de plomo. Sin embargo, en la actualidad la normativa medioambiental prohíbe y limita su utilización, disminuyendo bastante dichas emisiones con el uso creciente de gasolina sin plomo.
Límites
LEGISLACIÓN
Real Decreto 1073/2002, de 18 de octubre, sobre evaluación y gestión de la calidad del aire ambiente en relación con el dióxido de azufre, dióxido de nitrógeno, óxidos de nitrógeno, partículas, plomo, benceno y monóxido de carbono. Concretamente para el plomo, transpone la Directiva 1999/30/CE.
Valor límite para el plomo expresado en µg/m³
| Periodo de promedio | 2000 | 2001 | 2002 | 2003 | 2004 | 2005 | |
| Valor límite para la protección de la salud humana | 1 año civil | 1 | 0.9 | 0.8 | 0.7 | 0.6 | 0.5 |
Real Decreto 1073/2002, de 18 de octubre, sobre evaluación y gestión de la calidad del aire ambiente en relación con el dióxido de azufre, dióxido de nitrógeno, óxidos de nitrógeno, partículas, plomo, benceno y monóxido de carbono. Concretamente para el plomo, transpone la Directiva 1999/30/CE.
Valor límite para el plomo expresado en µg/Nm³
| Periodo de referencia | Valor límite |
| Anual | 2 - Media aritmética de los valores medios diarios registrados durante el año de referencia |
Monóxido de Carbono
Ficha técnica
Es un compuesto incoloro, inodoro y su punto de ebullición es de -192 ºC. Es un gas muy ligero, poco soluble en agua e inflamable a elevadas temperaturas.
Su vida media en la atmósfera es corta y abunda en la troposfera sobre todo en zonas urbanas e industriales, debido a que se genera principalmente como resultado de la combustión incompleta de combustibles fósiles.
Es tóxico a concentraciones elevadas y contribuye indirectamente al calentamiento global como precursor del ozono.
Efectos
Salud
El Monóxido de carbono afecta a la salud por su capacidad de combinarse con la hemoglobina de la sangre, reduciendo la capacidad de ésta para transportar oxígeno. La aparición de niveles altos de Monóxido de carbono sólo pueden producirse en ambientes cerrados, dándose en el aire ambiente bajas concentraciones de este contaminante.
Medio Ambiente
Como precursor el dióxido de carbono y del ozono, el CO contribuye al calentamiento global del planeta (efecto invernadero). También contribuye a los efectos directos del ozono sobre la vegetación y los materiales.
Fuentes
En un principio se pensó que las emisiones de CO eran casi exclusivamente del hombre pero más tarde se demostró la existencia de fuentes naturales de CO.
Naturales
Entre los procesos naturales de producción de CO están:

- La oxidación atmosférica del metano (CH₄) procedente de la fermentación anaerobia (sin aire) de la materia orgánica.
- La acción volcánica.
- Descargas eléctricas de tormentas.
- Incendios forestales.
- Emisiones de gas natural.
Se calcula que alrededor de un tercio del CO atmosférico se genera por fuentes naturales.
Antropogénicas

Las emisiones por parte del hombre tienen mayor importancia debido a que éstas se concentran en zonas localizadas pudiendo provocar efectos nocivos sobre la población.
Hoy en día, el principal problema de contaminación atmosférica por CO es debida a fuentes antropogénicas, debido a la combustión incompleta de carburantes en los automóviles. La concentración en el aire de este gas se ve influenciada por el volumen de tránsito y el clima local.
Otras fuentes antropogénicas de CO son:
- Las quemas de residuos agrícolas.
- El uso de combustibles fósiles.
- La generación de energía eléctrica mediante centrales Térmicas.
Formación
La formación del monóxido de carbono en la atmósfera por actividades humanas generalmente es debida a alguno de los tres procesos siguientes:
- Mediante la combustión del carbono de los carburantes. Esto ocurre en dos etapas:
- 2C + O₂ <--> 2CO
- 2CO + O₂ <--> 2 CO₂
- La generación de CO en la atmósfera es debida a la oxidación incompleta del carbono por una de las siguientes causas:
- Que la primera reacción sea más rápida que la segunda.
- Que no hay insuficiente oxígeno disponible en la atmósfera para completar la segunda reacción.
- Que existiendo suficiente oxígeno disponible, la mezcla de carburante y de aire no sea la correcta.
- En condiciones apropiadas, una reacción que tenga suficiente oxígeno para que la combustión sea completa puede así y todo actuar como fuente de CO, debido a la disociación del CO₂ a altas temperaturas.
- CO₂ <--> CO + ½ O₂
- Por reacción del CO₂ con el C que contienen algunos materiales.
- CO₂ + C <--> 2 CO
- Esta reacción ocurre a elevadas temperaturas y es frecuente en muchos procesos industriales tales como altos hornos.
- Disociación del CO₂ a altas temperaturas.
Límites
LEGISLACIÓN
Real Decreto 1073/2002, de 18 de octubre, sobre evaluación y gestión de la calidad del aire ambiente en relación con el dióxido de azufre, dióxido de nitrógeno, óxidos de nitrógeno, partículas, plomo, benceno y monóxido de carbono. Concretamente para el monóxido de carbono, transpone la Directiva 2000/69/CE.
El R.D. establece los valores indicados a continuación.
Valor límite para el monóxido de carbono expresado en mg/m³
| Periodo de promedio | 2000 | 2001 | 2002 | 2003 | 2004 | 2005 | |
| Valor límite para la protección de la salud humana | Media de ocho horas máxima en un día | 16 | 16 | 16 | 14 | 12 | 10 |
El Decreto 833/1975, de 6 de febrero, desarrolla la Ley 38/72 de Protección del Ambiente Atmosférico y establece los siguientes valores: (Valores derogados el 1 de Enero de 2005 por el Real Decreto 1073/2002)
Valores admisibles para el monóxido de carbono expresado en mg/m³N
| Periodo de referencia | Valores admisibles |
| 30 minutos | 45 (Concentración máxima) |
| 8 horas | 15 (Concentración media) |
Valores de emergencia para el monóxido de carbono expresado en mg/m³N
| Periodo de referencia | Valores de Emergencia | ||
| 1º grado | 2º grado | 3º grado | |
| 24 horas | 34 | 46 | 60 |
Hidrocarburos
Ficha técnica
HIDROCARBUROS (HₓCy)
Son compuestos orgánicos formados exclusivamente por carbono e hidrógeno. El estado físico de los hidrocarburos depende de su estructura molecular y en particular del número de átomos de carbono que forman su molécula.
Son gases importantes desde el punto de vista de la contaminación atmosférica, ya que favorecen la formación de reacciones fotoquímicas. Los hidrocarburos son contaminantes primarios que se oxidan en la troposfera en presencia de oxígeno atómico (O), el radical hidroxilo (OH) y ozono (O₃) para formar contaminantes secundarios.
HIDROCARBUROS GASEOSOS TOTALES (HCT)
En cuanto a los Hidrocarburos en general, el Decreto 833/75 establece unos criterios de calidad del aire para estos compuestos, expresados como n-hexano.
De esta manera, se establecen mediciones de los Hidrocarburos gaseosos totales (HCT) para determinar si los valores de concentración de estos compuestos en la atmósfera alcanzan los valores marcados como situación admisible.
METANO (CH₄)
De formula química CH₄, el metano es el hidrocarburo más abundante en la atmósfera. Su principal sumidero es el radical hidroxilo presente en la atmósfera.
El metano se oxida dando lugar a CO₂ y vapor de agua, gases de importante:
- Efecto Invernadero
HIDROCARBUROS GASEOSOS NO METÁNICOS (HNM)
Aparecen otros grupos de hidrocarburos en atmósferas urbanas los cuales se resumen agrupados a continuación:
| Grupo | Compuesto | |
| HC. alifáticos | Alcanos | Etano |
| Hexano | ||
| Alquenos | Eteno | |
| Propeno | ||
| Isopropeno | ||
| Alquinos | Acetileno | |
| HC. aromáticos | Benceno | |
| Tolueno | ||
| Xileno | ||
Efectos
Vegetación
Los hidrocarburos que provienen de la atmósfera al depositarse en la superficie del suelo quedan retenidos, alterando las características del mismo, y por tanto, pueden afectar a la vegetación que se desarrolla en dicho suelo.
Los hidrocarburos ocasionan daños indirectos por su capacidad para crear radicales libres a partir de una reacción con el radical hidroxilo (OH) y su posterior participación en reacciones productoras de:
- Ozono troposférico
- Peroxoacetilnitratos
- Otros contaminantes secundarios relacionados con el 'smog fotoquímico'
Salud
Los compuestos aromáticos, cuando se inhalan en gran cantidad pueden ocasionar trastornos en el sistema respiratorio irritando las membranas mucosas. Estos compuestos aromáticos y sus productos de oxidación son además precursores de partículas finas en áreas urbanas.
Uno de los hidrocarburos más representativos es el benceno, sobre el cual se han adoptado medidas legislativas específicas para el control de su presencia en el atmósfera.
Fuentes
Realizamos una distinción dentro de las fuentes atendiendo a los diferentes grupo de hidrocarburos que hemos considerado.
FUENTES DE METANO (CH₄)
Naturales
El metano (CH₄) es el hidrocarburo emitido a la atmósfera en mayor cantidad. Su concentración es anormalmente elevada, lo cual se debe a su considerable producción natural en la descomposición bacteriana anaerobia de la materia orgánica y a su desprendimiento en zonas geotérmicas, depósitos de carbón, gas natural y pozos de petróleo. Todo esto lleva a concentraciones elevadas de este gas en la atmósfera y una vida media para este compuesto de unos veinte años.
Antropogénicas
Casi la mitad del metano expedido a la atmósfera se puede relacionar con las actividades humanas, tal y como se indica a continuación:
- Plantaciones agrícolas como el cultivo de arroz.
- Explotaciones ganaderas.
- Escapes de biogás en vertederos de residuos.
- Procesos de explotación de actividades mineras carboníferas.
- Procesos de combustión, especialmente en motores de vehículos.
FUENTES DE HIDROCARBUROS NO METÁNICOS (HNM)
Naturales
También se producen hidrocarburos de este tipo a partir de la actividad metabólica de la vegetación (principalmente isopreno y monoterpenos), y a partir de la actividad microbiana.
Antropogénicas
La mayor parte de hidrocarburos considerados en este apartado proceden principalmente de diferentes escapes de los vehículos de motor.
Existen diversos hidrocarburos, como el n-Hexano, el Benceno, el Tolueno y el Xileno que se utilizan comúnmente como disolventes en la industria del mueble y en la fabricación de pinturas y barnices.
Límites
LEGISLACIÓN
Real Decreto 1073/2002, de 18 de octubre, sobre evaluación y gestión de la calidad del aire ambiente en relación con el dióxido de azufre, dióxido de nitrógeno, óxidos de nitrógeno, partículas, plomo, benceno y monóxido de carbono. Concretamente para el Benceno, transpone la Directiva 2000/69/CE.
El R.D. establece los valores indicados a continuación.
Valor límite para el benceno, expresado en µg/m³
| Periodo de promedio | 2000 | 2001 | 2002 | 2003 | 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | |
| Valor límite para la protección de la salud humana | Año Civil | 10 | 10 | 10 | 10 | 10 | 10 | 9 | 7 | 8 | 6 | 5 |
El Decreto 833/1975, del 6 de febrero, desarrolla la Ley 38/72 de Protección del Ambiente Atmosférico y establece los valores indicados a continuación. (Valores derogados el 1 de Enero de 2005 por el Real Decreto 1073/2002)
Valores admisibles para los hidrocarburos (expresado como n-hexano) en mg/m³
| Tiempo Promedio | Concentración Media |
| 24 horas | 140 |
| 30 minutos | 280 |
Metales (As, Ni, Cd)
Ficha técnica
Metales (Arsénico, Níquel, Cadmio)
Las partículas en suspensión existentes en el aire ambiente, pueden contar con la presencia de diferentes metales en su composición. Atendiendo a la presencia de unos u otros metales en superficie, y de la concentración de éstos, tendrán diferentes efectos sobre la salud y sobre el medio ambiente. Los efectos de dichos metales se producen tanto a través de la concentración de éstos en el aire como por su depósito al ser transferidos de la atmósfera a las superficies.
Efectos
Salud
La Directiva 2004/107/CE, afirma lo siguiente en relación a los efectos que los metales pueden tener:
"Los datos científicos muestran que el arsénico, el cadmio, el níquel y algunos hidrocarburos aromáticos policíclicos son cancerígenos genotóxicos para el ser humano y que no hay ningún límite identificable por debajo del cual esas substancias no constituyan un riesgo para la salud humana."
En relación al Mercurio, dicha Directiva establece lo siguiente:
"El mercurio es una substancia muy peligrosa para la salud humana y el medio ambiente. Está presente por todas partes en el medio ambiente y, en forma de metilmercurio, tiene la capacidad de acumularse en organismos y, en particular, de concentrarse en organismos al final de la cadena alimentaria. El mercurio liberado a la atmósfera es capaz de ser transportado a grandes distancias."
Vegetación
La deposición de metales en el suelo, donde éstos se encuentran como elementos traza (en concentraciones muy bajas), cuando ésta supone un incremento de la concentración de metales, puede producir condiciones de toxicidad para la presencia y el desarrollo de la vegetación. La presencia de metales en concentraciones elevadas en los suelos pueden producir necrosis en la vegetación, así como inhibición en el crecimiento de las plantas.
Fuentes
Naturales
Los metales que se encuentran formando parte de los suelos, como elementos traza, pueden pasar a la atmósfera por resuspensión de las partículas que forman dichos suelos, así como por erupciones volcánicas, aunque estos procesos no afectan de manera importante a la concentración de éstos en el aire ambiente.
Antropogénicas
Atendiendo a la naturaleza del metal, las fuentes emisoras son diferentes. Las principales actividades emisoras de los metales descritos con anterioridad son:
- Procesos de incineración de residuos.
- Operaciones de extracción, fundición, refinado y uso de metales.
- Procesos de combustión debidos al tráfico y a las centrales térmicas.
Formación
En cuanto a los metales, no se produce un proceso de formación, sino que se trata de substancias naturales que se encuentran formando parte de la corteza terrestre, y también de manera natural en el ambiente, como en el caso del mercurio, en forma de mercurio metálico o compuestos de mercurio.
Límites
LEGISLACIÓN
Directiva 2004/107/CE del Parlamento Europeo y del Consejo, de 15 de diciembre de 2004, relativa al arsénico, el cadmio, el mercurio, el níquel y los hidrocarburos policíclicos en el aire ambiente.
La directiva mencionada establece unos valores objetivo de concentración de metales como el cadmio, arsénico y níquel en el aire ambiente, los cuales serán aplicables a partir del 31 de diciembre de 2012. Dichos valores se resumen en la siguiente tabla:
| Contaminante | Valor objetivo (1) |
| Arsénico | 6 ng/m³ |
| Cadmio | 5 ng/m³ |
| Níquel | 20 ng/m³ |
(1) Referente al contenido total en la fracción PM₁₀ como promedio en un año natural.
Óxidos de Nitrógeno
Ficha técnica
Los compuestos nitrogenados más importantes, desde el punto de vista de la contaminación atmosférica, son los óxidos de nitrógeno. Se conocen ocho óxidos de nitrógeno distintos, y en la atmósfera podemos encontrarlos en tres formas, como óxido nitroso (N₂O), óxido nítrico (NO) y como dióxido de nitrógeno (NO₂). De éstos, solo se consideran contaminantes el NO y el NO₂, formados en los procesos de combustión a partir de la oxidación del nitrógeno atmosférico. El resto se encuentra en equilibrio con estos tres y en concentraciones tan bajas que carecen de importancia.
- Óxido nitroso (N2O)
- Gas incoloro, no inflamable ni tóxico.
- Es el óxido de nitrógeno más abundante en la baja atmósfera.
- Es fuente primaria de otros óxidos de nitrógeno causantes de nieblas de contaminación fotoquímica ('smog fotoquímico')
- Óxido nítrico (NO)
- Gas incoloro, inodoro, no inflamable y tóxico por su capacidad para oxidarse a NO₂.
- Dióxido de nitrógeno (NO₂)
- Gas de tonalidad rojiza, de fuerte olor, no inflamable, muy corrosivo y tóxico (cuatro veces mas tóxico que el NO).
- De los tres es el más importante por sus efectos sobre la salud humana.
- Interviene en la formación de la niebla fotoquímica.
- En la atmósfera puede reaccionar con agua dando lugar al proceso de 'acidificación del medio'
Efectos
El dióxido de nitrógeno (NO₂) es, de los óxidos de nitrógeno, el más importante por sus efectos sobre la salud y sobre la vegetación cuando se encuentra en la atmósfera a altas concentraciones.
Salud
A elevadas concentraciones puede, en periodos de larga exposición, producir los siguientes efectos:
- Alteraciones sobre el sistema respiratorio: tos, fatiga.
- Irritación ocular: conjuntivitis.
Vegetación
El nitrógeno es un nutriente esencial para las plantas que en concentraciones normales favorece el crecimiento, sin embargo elevadas concentraciones pueden fomentar efectos adversos originando daños en los ecosistemas, pudiendo producir los siguientes efectos:
- Una reducción del crecimiento vegetal.
- La aparición de necrosis y clorosis en las hojas.
Medio Ambiente
Los óxidos de nitrógeno (NOₓ) contribuyen de manera importante en el desarrollo de fenómenos como la 'acidificación del medio' y el 'smog fotoquímico'.
Los óxidos de nitrógeno (NOₓ) junto con los compuestos orgánicos volátiles (COV) reaccionan en presencia de la luz solar y contribuyen a la formación de una serie de compuestos conocidos como oxidantes fotoquímicos. El oxidante fotoquímico más importante por su abundancia y toxicidad es el ozono troposférico (O₃), que junto con los PeroxiAcetilNitratos (PAN) es uno de los principales causantes del fenómeno conocido como "smog fotoquímico".
Por otra parte, los óxidos de nitrógeno en concentraciones elevadas también pueden contribuir a la eutrofización en las zonas costeras.
Fuentes
Naturales
Los óxidos de nitrógeno se presentan de forma natural en el atmósfera como consecuencia de:
- Las erupciones volcánicas.
- Las tormentas.
- La desnitrificación de los suelos.
- Incendios forestales.
El óxido nitroso (N₂O) procede en casi su totalidad de la descomposición de compuestos nitrogenados debido a la actividad bacteriana. Parte del amoniaco que existe en el suelo se oxida a NO₂ por medio de bacterias autótrofas pero otra parte no se oxida, sino que pasa a N₂O. Estos procesos se ven incrementados por el uso excesivo de derivados amoniacales y de urea, que aportan el estiércol animal y los fertilizantes, procedentes del sector agrícola y ganadero.
Antropogénicas
Las principales fuentes antropogénicas de NOₓ son:
- El transporte.
- La utilización de combustibles fósiles, en la generación de electricidad y en los procesos industriales (cementeras, incineradoras, etc.)
Otras fuentes de emisión de óxidos de nitrógeno son: las refinerías, calefacciones, fábricas de fertilizantes, quemas agrícolas, etc.
Formación
El nitrógeno y el oxígeno son dos gases que se encuentran en la atmósfera de forma natural. A temperatura ambiente el nitrógeno no reacciona fácilmente con el oxígeno debido a su poca reactividad química (por eso el aire mantiene como una mezcla de nitrógeno y oxígeno, principalmente). Sin embargo, en condiciones de elevadas temperaturas (aproximadamente 1000ºC) se produce la reacción indicada a continuación.
- N₂ + O₂ --> 2NO
El óxido nítrico (NO) producido reacciona con el oxígeno (O₂) dando lugar al dióxido de nitrógeno (NO₂), uno de los principales responsables del 'smog fotoquímico'.
- 2NO + O₂ --> 2 NO₂
El dióxido de nitrógeno (NO₂) absorbe energía en forma de radiación ultravioleta procedente del sol. Esta energía rompe las moléculas de NO2 para dar moléculas de NO y átomos de oxígeno (O).
- NO₂ + hv --> NO + O
Los átomos de oxígeno producidos, que son muy reactivos, reaccionan con las moléculas de oxígeno atmosférico (O₂) dando lugar al ozono (O₃).
- O + O₂ --> O₃
El ozono (O₃) al igual que los demás peróxidos es muy reactivo y reacciona con el óxido nítrico (NO) produciendo dióxido de nitrógeno (NO₂) y oxígeno molecular.
- O₃ + NO --> NO₂ + O₂
Por otra parte, el dióxido de nitrógeno (NO₂) puede combinarse con agua (H₂O) produciendo ácido nítrico (HNO₃) y óxido nítrico (NO) o una mezcla de ácido nítrico (HNO₂), según la cantidad de dióxido de nitrógeno que reaccione con la misma. Estas reacciones son las que dan lugar al efecto conocido como:
- 'Acidificación del medio'
- 3 NO₂ + H₂O --> 2 HNO₃ + NO
- 2 NO₂ + H₂O --> HNO₃ + HNO₂
Límites
LEGISLACIÓN
Real Decreto 1073/2002, de 18 de octubre, sobre evaluación y gestión de la calidad del aire ambiente en relación con el dióxido de azufre, dióxido de nitrógeno, óxidos de nitrógeno, partículas, plomo, benceno y monóxido de carbono. Concretamente para el dióxido de nitrógeno y óxidos de nitrógeno, transpone la Directiva 1999/20/CE.
Este R.D. establece unos Valores límite para el dióxido de nitrógeno y los óxidos de nitrógeno, así como un Umbral de alerta para el dióxido de nitrógeno. Dichos valores se resumen a continuación.
Valores límite del dióxido de nitrógeno y de los óxidos de nitrógeno, expresados en µg/m³
| Periodo de promedio | 2000 | 2001 | 2002 | 2003 | 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | |
| Valor límite horario para la protección de la salud humana | 1 hora. No podrá superarse en más de 18 ocasiones por año civil. (NO₂) | 300 | 290 | 280 | 270 | 260 | 250 | 240 | 230 | 220 | 210 | 200 |
| Valor límite para la protección de la salud humana | Año civil. NO₂ | 60 | 58 | 56 | 54 | 52 | 50 | 48 | 46 | 44 | 42 | 40 |
| Valor límite para protección de la vegetación | Año civil. NOₓ | 30 | ||||||||||
Umbral de alerta del dióxido de nitrógeno
| Periodo de promedio | Umbral de alerta del NO₂ |
| 3 horas consecutivas en lugares representativos de la calidad del aire | 400 µg/m³ |
En lo que se refiere al dióxido de nitrógeno, NO₂, el Real Decreto 717/1987, de 27 de mayo, por el que se modifica parcialmente el Decreto 833/1975, de 6 de febrero, y se establecen nuevas normas de calidad del aire en lo referente a contaminación por dióxido de nitrógeno y plomo, que es la transposición al derecho español de la Directiva 85/203/CEE establece los valores límite y guía para el dióxido de nitrógeno.
Valor límite para el dióxido de nitrógeno expresado en µg/m³
| Periodo de referencia | Valores límite |
| Anual (compuesto por unidades de periodos de una hora o menos) | 200. Percentil 98, calculado a partir de valores medios por hora, o periodos inferiores a la hora, tomados a lo largo de todo el año. |
Para reconocer la validez del cálculo del percentil 98 es necesario disponer del 75% de los valores posible, y que, dentro de lo posible, estos se hallen repartidos uniformemente en el conjunto del año considerado.
Valores guía para el dióxido de nitrógeno expresado en µg/m³
| Periodo de referencia | Valores guía |
| Anual (compuesto por unidades de períodos de una hora o menos) | 50. Percentil 50 calculado a partir de los valores medios por hora o por períodos inferiores a una hora, tomados a lo largo de todo el año. |
| 135. Percentil 98 calculado a partir de los valores medios por hora o por períodos inferiores a una hora, tomados a lo largo de todo el año. |
Para reconocer la validez del cálculo del percentil 98 es necesario disponer del 75% de los valores posible, y que, dentro de lo posible, estos se hallen repartidos uniformemente en el conjunto del año considerado.
En el Real Decreto 717/1987 también se establecen los valores de referencia para la declaración de la situación de emergencia por dióxido de nitrógeno, como se resume a continuación.
Valores de emergencia para el dióxido de nitrógeno expresado en µg/m³
| Periodo de referencia | Valores de Emergencia | ||
| 1º grado | 2º grado | 3º grado | |
| 1 hora | 975 | 1270 | 1700 |
| 24 horas | 565 | 750 | 1000 |
| 7 días | 409 | 543 | 724 |
Dióxido de Azufre
Ficha técnica
El dióxido de azufre es un gas bastante estable, incoloro, no inflamable y muy soluble en agua. En altas concentraciones tiene un olor fuerte e irritante. Es 2,2 veces más pesado que el aire, a pesar de lo cual se desplaza rápidamente en la atmósfera, y su vida media es de 2 a 4 días.
Efectos
El dióxido de azufre (SO₂) es uno de los principales contaminantes que, junto con el óxido nítrico (NOₓ) y el amoniaco (NH₃), forma parte de los procesos de acidificación.
Salud
El dióxido de azufre puede causar, en altas concentraciones, irritación de ojos, mucosas y piel, aunque raras veces se llega a concentraciones elevadas.
Vegetación

Los efectos en la vegetación varían dependiendo de la concentración de dióxido de azufre en la atmósfera y del tiempo al que están expuestas las plantas, aunque también pueden influir la temperatura, la humedad y la sinergia con otros contaminantes.
Los principales efectos en la vegetación son el amarilleo de las hojas, necrosis y caída de las mismas.
El SO₂ entra directamente al interior de las hojas a través de los estomas, donde la planta lo transforma a formas asimilables para su metabolismo. Una concentración elevada de SO₂ impide que dicha transformación se produzca con suficiente velocidad e inicia la ruptura celular.
La sensibilidad de los distintos tipos de plantas a la exposición al SO₂ en la atmósfera varía considerablemente, siendo los líquenes los más fácilmente afectados.
Materiales
Un alto contenido de SOₓ en la atmósfera causa daños a muchos tipos de materiales, bien directa o indirectamente, provocando la corrosión de metales tales como el acero, zinc, compuestos de cobre, níquel y aluminio.
Las nieblas de ácido sulfúrico procedentes de la conversión catalítica del SO₂ y SO₃ en la atmósfera, atacan a materiales de construcción como el mármol, la caliza y la piedra arenisca, provocando la degradación de patrimonios histórico-artístico.
El SO₂ también es responsable de la degradación de otro tipo de materiales como el cuero y el papel, proceso ligado a la formación de SO₃ y H₂SO₄, que provoca en última instancia la hidrólisis de celulosa y de las proteínas del cuero.
Los daños en los materiales dependen de condiciones meteorológicas y de factores de contaminación, originándose mayores daños en zonas industrializadas, ya que se han observado correlaciones entre tasas de corrosión en metales y concentraciones de SO₂ en la atmósfera.
Fuentes
Naturales
La única fuente natural de SO₂ procede de la actividad volcánica, de las fumarolas, géisers, etc., y también de diferentes procesos biológicos que se desarrollan en los océanos y en los suelos. Estos pueden dar lugar a SO₂ (como la oxidación de compuestos de azufre en la descomposición de plantas) o a SH₂, que posteriormente en la atmósfera se oxida a SO₂.
Antropogénicas
Las principales fuentes de emisión son las indicadas a continuación:
- La combustión de carbón y petróleo en procesos industriales.
- Operaciones de refinado del petróleo.
- Metalurgia, se produce en la obtención de metales a partir de sulfuros metálicos, a excepción del sulfuro de hierro, a partir del cual se extrae el azufre.
- El transporte.
- Las centrales térmicas como fuentes puntuales de SO₂.
Formación
Los combustibles fósiles (carbón y derivados del petróleo), así como los sulfuros metálicos, presentan azufre (S) en su composición, se combina con el oxígeno (O₂) dando lugar al dióxido de azufre (SO₂) en la atmósfera.
- S + O₂ --> SO₂
En la atmósfera también se encuentra en menor proporción (1-2% de los óxidos de azufre) anhídrido sulfúrico, SO₃, un gas incoloro y muy reactivo que en condiciones normales reacciona rápidamente con el agua atmosférica formando ácido sulfúrico. El SO₃ también se forma por la combinación del azufre de los combustibles con el oxígeno en los procesos de combustión. La cantidad producida va a depender de las condiciones de reacción, especialmente de temperatura, en dichos procesos de combustión.
- SO₃ + H₂O --> H₂SO₄
Límites
LEGISLACIÓN
Real Decreto 1073/2002, de 18 de octubre, sobre evaluación y gestión de la calidad del aire ambiente en relación con el dióxido de azufre, dióxido de nitrógeno, partículas, plomo, benceno y monóxido de carbono. Concretamente para el dióxido de azufre transpone la Directiva 1999/30/CE.
Este R.D. establece valores límite y un umbral de alerta para el dióxido de azufre, como se resume a continuación.
Valor límite para el dióxido de azufre, expresado en µg/m³
| Periodo de promedio | 2000 | 2001 | 2002 | 2003 | 2004 | 2005 | |
| Valor límite horario para la protección de la salud humana | 1 hora. No podrá superarse en más de 24 ocasiones por año. | 500 | 470 | 440 | 410 | 380 | 350 |
| Valor límite diario para la protección de la salud humana | 24 horas. No podrá superarse en más de 3 ocasiones por año. | 125 | |||||
| Valor límite para la protección de los ecosistemas | Año civil e invierno (1 de octubre a 31 de marzo) | 20 | |||||
Umbral de alerta del dióxido de azufre
| Periodo de promedio | Umbral de alerta del SO₂ |
| 3 horas consecutivas en lugares representativos de la calidad del aire | 500 µg/m³ |
El Real Decreto 1321/1992, de 30 de octubre, que modifica al Real Decreto 1613/1985, establece los siguientes valores límite para el dióxido de azufre. (Valores derogados el 1 de Enero de 2005 por el Real decreto 1073/2002).
Valores límites para el dióxido de azufre y valores asociados para las partículas en suspensión, expresado en µg/m³
| Periodo considerado | Valor límite para el Dióxido de Azufre | Valor asociado para las partículas en suspensión | |
| Método del humo normalizado | Método gravimétrico | ||
| Anual | 80 | >40 | >150 |
| 120 | ≤40 | ≤150 | |
| Medianas de los valores medios diarios registrados durante el periodo anual | |||
| Invernal | 130 | >60 | >200 |
| 180 | ≤60 | ≤200 | |
| Medianas de los valores medios diarios registrados durante el periodo invernal | |||
| Anual | 250* | >150 | >350 |
| 30* | ≤150 | ≤350 | |
| * No deben sobrepasar durante más de tres días consecutivos Percentil 98 de todos los valores medios diarios registrados durante el periodo anual | |||
El Real Decreto 1613/1985, de 1 de agosto, establece valores guía para el dióxido de azufre. También establece valores de referencia para la declaración de situación de emergencia, para el producto de concentraciones de SO₂ y partículas en suspensión. Los valores se resumen en las tablas indicadas a continuación. (Valores derogados el 1 de Enero de 2005 por el Real Decreto 1073/2002).
Valores guía para el dióxido de azufre expresado en µg/m³N
| Periodo considerado | Valores guía |
| Anual | 40-60. Media aritmética de los valores medios diarios registrados durante el año |
| 24 horas | 100-150. Valor medio diario |
Valores de referencia para la declaración de la situación de emergencia de SO₂ y partículas en suspensión, expresado en µg/m³N
| Periodo de referencia | Valores de Emergencia | ||
| 1º grado | 2º grado | 3º grado | |
| 1 día | 160 x 10³ | 300 x 10³ | 500 x 10³ |
| 3 día | 125 x 10³ | 250 x 10³ | 420 x 10³ |
| 5 día | 115 x 10³ | 230 x 10³ | |
| 7 día | 110 x 10³ | ||
Ozono
Ficha técnica
El ozono es un gas incoloro de olor algo fresco que posee un gran poder oxidante. Constituye el 10% de todo el ozono atmosférico y debido a los procesos químicos que transcurren en áreas urbanas industrializadas, los niveles de ozono pueden aumentar significativamente, alcanzándose niveles a partir de los cuales se pueden originar efectos sobre los seres vivos y los materiales.
Se forma en la troposfera por acción de la luz solar sobre los gases considerados como sus precursores, siendo los más importantes los óxidos de nitrógeno (NOₓ), compuestos orgánicos volátiles (COV), el monóxido de carbono (CO) y el metano (CH₄). Es por tanto un contaminante secundario, ya que no es emitido directamente a la atmósfera por ninguna fuente y, también, un contaminante fotoquímico, ya que se forma con la intervención de la luz solar.
Por otra parte, el ozono troposférico absorbe la radiación infrarroja potenciando el efecto invernadero y a concentraciones altas es el componente más dañino del smog fotoquímico.
La Conselleria de Medio Ambiente de la Generalitat Valenciana, con la colaboración de la Fundación Centro de Estudios Ambientales del Mediterráneo (CEAM) desarrolla, dentro del marco de las directivas europeas sobre contaminación atmostérica, una campaña estival de vigilancia de los niveles de contaminación por ozono en la atmósfera, Previozono 2002 con objeto de informar sobre los niveles diarios de ozono y prevenir a la población sobre posibles casos de superación de los valores umbrales.
| EFECTO INVERNADERO |
|---|
EL EFECTO INVERNADERO Durante las últimas décadas, se ha incrementado la preocupación acerca de los efectos sobre el clima que puede tener una creciente emisión de contaminantes a la atmósfera por parte de las actividades humanas. La temperatura media de la superficie terrestre se mantiene constante, ya que en el balance térmico terrestre, la cantidad de energía que llega a la superficie es igual a la energía que se desprende de ésta. Podemos definir como 'Efecto Invernadero' al fenómeno mediante el cual algunos gases existentes en la troposfera, como el dióxido de carbono, vapor de agua, metano, óxido nitroso y algunos compuestos halogenados, retienen parte de las radiaciones de baja frecuencia que son remitidas hacia el exterior por parte de la superficie terrestre. Este efecto es el responsable de que la temperatura media en la superficie terrestre sea de unos 15°C. Sin la presencia de estos gases de efecto invernadero la temperatura media en superficie sería de unos -18°C, y no sería posible la existencia de vida tal y como la conocemos en la actualidad. La creciente concentración de este tipo de gases de efecto invernadero, debido a diversas actividades por parte del hombre, produce una mayor absorción de la radiación infrarroja emitida desde la superficie terrestre, con un posterior aumento de la temperatura.
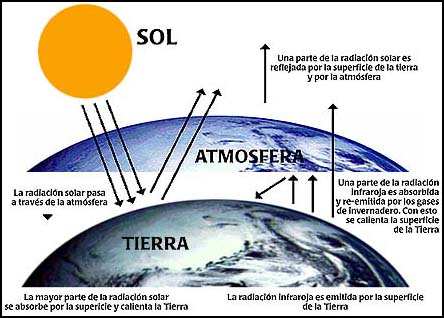
La contribución relativa de las emisiones de contaminantes a las alteraciones del clima es tema central de las investigaciones que se desarrollan en la actualidad, para así conocer los posibles efectos a escala planetaria que pudieran derivarse de las actividades humanas.
Fuente de los gases invernaderos  El dióxido de carbono se encuentra de forma natural en la atmósfera en una concentración constante debido al ciclo del carbono, pero se ve alterado por las actividades del hombre que hacen que este gas aumente de forma considerable. Las actividades que más afectan al incremento de las emisiones de CO₂, son el aumento del uso de combustibles fósiles, la fabricación de cemento, los procesos de tratamiento de carburantes y fugas en explotaciones mineras. Hoy en día el aumento de los niveles de dióxido de carbono es sobre todo por la quema de combustibles fósiles en países industrializados, ya que se ha comprobado que por cada kilogramo de combustible que se consume se produce alrededor de unos tres kilogramos de dióxido de carbono. La existencia de incendios, que generan a su vez gran cantidad de CO₂, y la tala progresiva de bosques, son dos importantes factores que favorecen la degradación de los suelos y la creciente desertificación. El problema de la disminución de masas forestales produce, a su vez, una gran disminución de la tasa de absorción total de CO₂ debida a la vegetación. Esta disminución de los sumideros de gases de efecto invernadero acentúa la problemática del cambio climático.
Consecuencias del efecto invernadero
Según el segundo informe publicado por el IPCC (Intergovernamental Panel on Climate Change) en 1995, se estima un aumento de la temperatura media global del aire en el año 2100 entre 1°C y 3,5°C. Un calentamiento de esta magnitud alteraría el clima en todo el mundo originando vientos más cálidos y secos. Esto provocaría en mayor o menor grado una serie de consecuencias, como un ascenso del nivel del mar por la fusión de hielos y glaciares (sobre todo en la Antártida), tormentas, inundaciones y sequías más intensas y frecuentes, así como cambios en la biota y en la productividad de alimentos. |
| EL SMOG FOTOQUÍMICO | ||||||||
|---|---|---|---|---|---|---|---|---|
Otra de las consecuencias de la contaminación atmosférica, es el fenómeno denominado 'Contaminación fotoquímica'. La producción de oxidantes fotoquímicos es un sistema complejo en el cual influye tanto la meteorología como las emisiones continuas de contaminantes y las reacciones que se producen entre ellas. De entre los procesos de formación de oxidantes fotoquímicos se puede resaltar la formación de ozono a través del ciclo fololítico del NO₂, la reacción del ozono y el oxígeno con hidrocarrburos produciendo radicales libres y la reacción de estos radicales libres primarios entre sí, produciendo otros contaminantes fotoquímicos. La mezcla de todas estas sustancias da lugar a la contaminación fotoquímica, denominada también 'smog fotoquímico'. Pequeñas cantidades de NO₂ son suficientes para producir la compleja serie de reacciones que supone el 'smog fotoquímico', el NO₂ se forma generalmente a parir del NO que se emite en los gases de combustión.
Este conjunto de reacciones podría alargarse añadiendo las reacciones que entre sí originarán los radicales libres formados y las reacciones de estos con los óxidos de nitrógeno y el ozono, etc... El 'smog fotoquímico' es la coexistencia de reactivos y productos en una atmósfera urbana, cuando tenemos óxidos de nitrógeno (NOₓ), monóxido de carbono (CO), metano (CH₄) y otros compuestos orgánicos volátiles (COVs), en presencia de radiación solar. La radiación que entra en juego es selectiva, con una longitud de onda umbral que provoca la reacción, y sin la cual la reacción no se produce. De la porción del espectro que alcanza la superficie terrestre, la banda ultravioleta y sus proximidades son las que intervienen en todos los procesos fotoquímicos, al ser las radiaciones más energéticas. De entre todos los productos del 'smog fotoquímico' se puede resaltar el ozono troposférico, los nitratos de peroxiacilo (PAN), aldehidos, cetonas, etc... Todos ellos importantes por lo que afectan en casos de afecciones asmáticas y broncopulmonares, y las lesiones foliares que originan en la plantas. Junto con el ozono troposférico, unos de los contaminantes secundarios más importantes originados en este proceso de contaminación fotoquímica son: |
| PEROXOACETILNITRATOS |
|---|
Los PeroxoAcetilNitratos (PAN) son contaminantes secundarios formados por reacción fotoquímica de los compuestos orgánicos volátiles (COV's) y los óxidos de nitrógeno (NOₓ). En el medio atmosférico, los COV's reaccionan con oxígeno, ozono o radicales libres con producción de alehídos. Estos aldehídos se degradan por medio de mecanismos en los que intervienen los óxidos de nitrógeno, con reacciones finales de formación de peróxidos (peroxiaceltilnitratos).
Los peroxiacetilnitratos son compuestos altamente irritantes y lacrimógenos. Producen efectos dañinos en la vegetación. Fuentes Naturales No se han identificado fuentes naturales. Fuentes Antropogénicas Es un contaminante secundario que aparece como consecuencia de reacciones fotoquímicas en una atmósfera contaminada, generalmente urbana, por hidrocarburos, en presencia de óxidos de nitrógeno y ozono. La mayoría de los hidrocarburos, precursores de los PAN, proceden de las combustiones incompletas de los combustibles fósiles realizadas en la industria, calefacciones domésticas y en los motores de combustión interna de los vehículos. |
Efectos
Un aumento de los niveles del ozono troposférico es motivo de inquietud por los efectos adversos que este compuesto puede ejercer sobre las personas, animales, vegetación y materiales.
Salud
Los efectos sobre la salud de los seres vivos varían en función de la concentración de ozono que hay en el ambiente, de la duración de la exposición y de la sensibilidad del individuo hacia el contaminante.
El ozono puede provocar irritación ocular (conjuntivitis seca y lacrimación) aunque es el aparato respiratorio el principal perjudicado por la acción de este compuesto (deterioro de la función pulmonar, aumento de la reactividad bronquial, ... etc).
La Directiva 2002/3/CE establece el valor de 180 mg/m³ (valor medio en una hora) como umbral de información a la población, nivel a partir del cual una exposición de breve duración supone un riesgo para la salud humana de los grupos de población especialmente de riesgo. También establece el valor 240 mg/m³ (como valor medio en una hora) como umbral de alerta a la población, por encima del cual existe un riesgo para la salud humana de la población en general, en caso de exposición de breve duración.
Vegetación
En las especies vegetales el ozono penetra a través de los estomas abiertos provocando daños foliares y pérdidas de producción.
En general los daños en las plantas atribuibles a la contaminación por ozono son:
- Daños foliares (clorosis, necrosis y caída de hojas).
- Disminución de la producción vegetal (menor rendimiento y calidad de los cultivos).
- Mayor predisposición de las plantas a ataques mortales por plagas de insectos o enfermedades.
Materiales
Las obras de arte pueden sufrir graves daños por la exposición prolongada al ozono debido al carácter oxidante del mismo. Éste también tiene efectos corrosivos sobre la pintura, los géneros textiles, cauchos y plásticos; no obstante, estos daños suelen ser limitados al ser materiales resistentes, tras haber sido tratados con medidas preventivas (incorporación de antioxidantes).
Fuentes
Naturales
Aproximadamente el 20% del ozono que existe en la troposfera proviene de la formación natural de este gas en la estratosfera.
Antropogénicas
Al ser el ozono un contaminante secundario se forma por acción de la luz solar sobre sus precursores, como son los óxidos de nitrógeno (NOₓ), compuestos orgánicos volátiles (COV), el monóxido de carbono (CO) y el metano (CH₄).
En los últimos años se ha observado un incremento de los precursores del ozono debido a la emisión incontrolada por parte del hombre de dichos compuestos. Los sectores que contribuyen mayoritariamente a la emisión de estos contaminantes primarios precursores del ozono son:

- Los procesos de combustión (el transporte y la generación de la energía eléctrica) y los procesos industriales son las fuentes más importantes de óxidos de nitrógeno (NOₓ).
- Los procesos que consumen combustibles fósiles (sólidos y gaseosos) y el uso de disolventes y pinturas son la principal fuente de compuestos orgánicos volátiles (COV).
El ozono es una molécula muy reactiva que sigue reaccionando con otros contaminantes presentes en el aire y acaba formando un conjunto de varias decenas de sustancias distintas como nitratos de peroxiacilo (PAN), peróxido de hidrógeno (H₂O₂), radicales hidroxilo (OH), formaldehído, etc.
Estas sustancias, en conjunto, pueden producir importantes daños, algunos de los cuales se describen a continuación.
Formación
Existen una serie de compuestos que intervienen en las reacciones que dan lugar a la formación de ozono. Estos son: los óxidos de nitrógeno (NOₓ), compuestos orgánicos volátiles (COV), el monóxido de carbono (CO) y el metano (CH₄).
Los COV y los NOₓ reaccionan de la siguiente manera:
COV₅ + OH + O₂ --> RO₂ + H₂O
RO₂ + NO + O₂ --> NO₂ + HO₂ + Compuestos de carbonillo
HO₂ + NO --> NO₂ + OH
2(NO₂ + hv + O₂ <--> NO + O₃)
----------------------------------------------------------------------------------------
(NOₓ + OH +) COV + 4O₂ --> 2O₃ + Compuestos de carbonillo + H₂O (+NOₓ + OH)
OH y HO₂ : Radicales
RO₂ : Hidrógenos peróxidos
Por su parte, los gases como el monóxido de carbono (CO) y el metano (CH₄) intervienen en la producción de ozono troposférico según el siguiente proceso:
CO + O₂ + hv --> ...... --> CO₂ + O₃ ----- λ < 410 nm
CH₄ + O₂ + hv --> ...... --> CO + O₃ + H₂O ----- λ < 330nm
Los niveles de ozono varían a lo largo del día, dependiendo de la intensidad del tráfico, de la actividad industrial y de la intensidad de la luz solar. Normalmente en los países mediterráneos es en verano (altas temperaturas, cielos despejados, elevada insolación y vientos bajos) cuando se dan condiciones meteorológicas favorables para la formación de ozono.
Límites
LEGISLACIÓN
En lo que se refiere al Ozono (O₃), la referencia normativa para el control de la calidad del aire viene indicada en el Real Decreto 1796/2003, de 26 de diciembre, relativo al ozono en el aire ambiente, que traspone al derecho español la Directiva 2002/3/CE del Parlamento europeo y del Consejo de 12 de febrero de 2002 relativa al ozono en el aire ambiente.
El Real Decreto 1796/2003, establece los siguientes valores objetivo y umbrales:
Valores objetivo de ozono
| Valor objetivo | Parámetro | Valor objetivo para 2010 |
| Valor objetivo para la protección de la salud humana | Máximo de las medias octohorarias del día | 120 µg/m³ que no deberá superarse más de 25 días por cada año civil de promedio en un período de 3 años |
| Valor objetivo para la protección de la vegetación | AOT40 calculada a partir de valores horarios de mayo a julio | 18000 µg/m³.h de promedio en un período de 5 años |
Valores objetivo a largo plazo de ozono
| Valor objetivo a largo plazo | Parámetro | Objetivo a largo plazo |
| Valor objetivo a largo plazo para la protección de la salud humana | Máximo de las medias octohorarias del día en un año civil | 120 µg/m³ utilizando como referencia el año 2020 |
| Valor objetivo a largo plazo para la protección de la vegetación | AOT40 calculada a partir de los valores de mayo a julio | 6000 µg/m³.h utilizando como referencia el año 2020 |
Umbrales de información y alerta relativos al ozono
| Parámetro | Umbral | |
| Umbral de información | Promedio horario | 180 µg/m³ |
| Umbral de alerta | Promedio horario * | 240 µg/m³ |
* A efectos del cumplimiento del artículo 7, la superación del umbral se debe medir o prever durante tres horas consecutivas.
Paginación
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- …
- Siguiente página
- Última página
 El efecto invernadero origina un aumento de la temperatura media de la tierra.
El efecto invernadero origina un aumento de la temperatura media de la tierra.